Masennus on Suomessa yleisin ja kansanterveyden kannalta merkittävin mielenterveyden häiriö (11 Suomalaisen Lääkäriseuran Duodecimin ja Suomen Psykiatriyhdistys ry:n asettama työryhmä. Depressio. Käypä hoito -suositus. (siteerattu 27.9.2021). www.kaypahoito.fi). Psykologisten ja sosiaalisten tekijöiden ohella masennuksen taudinkuvaan liittyy olennaisesti myös biologisia tekijöitä, kuten neurokemiallisen toiminnan ja aivojen rakenteen poikkeavuuksia (11 Suomalaisen Lääkäriseuran Duodecimin ja Suomen Psykiatriyhdistys ry:n asettama työryhmä. Depressio. Käypä hoito -suositus. (siteerattu 27.9.2021). www.kaypahoito.fi).
Masennukseen sairastuneiden aivoissa on aivokuvantamistutkimuksissa havaittu rakenteellisia poikkeavuuksia hippokampuksessa, useilla etuotsalohkon aivokuoren alueilla, pihtipoimun etu- ja takaosissa, aivosaaressa (insula), ohimolohkossa ja mantelitumakkeessa (2–4). Lisäksi poikkeavuuksia on havaittu useissa edellä mainittuja alueita yhdistävissä valkean aineen radastoissa, kuten aivokurkiaisen etuosassa sekä limbisissä (cingulum, fornix) ja ventraalisissa (inferior longitudinal fasciculus, ILF; inferior fronto-occipital fasciculus, IFOF) radastoissa (55 Van Velzen LS, Kelly S, Isaev D ym. White matter disturbances in major depressive disorder: a coordinated analysis across 20 international cohorts in the ENIGMA MDD working group. Mol Psychiatry 2020;25:1511–25.,66 Liao Y, Huang X, Wu Q ym. Is depression a disconnection syndrome? Meta-analysis of diffusion tensor imaging studies in patients with MDD. J Psychiatry Neurosci 2013;38:49–56.).
Rakenteellisten poikkeavuuksien pysyvyydestä ei ole vielä tarkkaa tietoa. On kuitenkin viitteitä siitä, että masennuksesta toipumiseen ja masennushoitoon liittyy korjaavia muutoksia aivojen rakenteessa. Näitä muutoksia käsitellään tässä artikkelissa.
Rakenteellisten poikkeavuuksien pysyvyydestä ei ole tarkkaa tietoa.
Masennuksen patogeneesiin ajatellaan liittyvän heikentymistä neuroplastisuudessa (77 Pittenger C, Duman RS. Stress, depression, and neuroplasticity: a convergence of mechanisms. Neuropsychopharmacology 2008;33:88–109.) eli aivojen kyvyssä muovautua toiminnallisesti ja rakenteellisesti muun muassa kasvun tai uudelleenjärjestäytymisen kautta. Masennukseen liittyvä pitkittynyt psyykkinen ja fysiologinen kuormitustila (stressi) heikentää aivojen muovautuvuutta muun muassa vähentämällä hermokasvutekijöiden synteesiä ja toimintaa, jota tarvitaan uusien synapsien muodostumiseen ja hermoverkostojen ylläpitämiseen (88 Duman RS, Aghajanian GK. Synaptic dysfunction in depression: potential therapeutic targets. Science 2012;338:68–72.).
Aivojen muovautuvuuden lisääntymisellä ajatellaan puolestaan olevan merkittävä rooli masennuksesta toipumisessa (99 Price RB, Duman R. Neuroplasticity in cognitive and psychological mechanisms of depression: an integrative model. Mol Psychiatry 2020;25:530–43.). Aivojen muovautuvuuteen vaikuttanut pitkittynyt kuormitustila voi lieventyä esimerkiksi vaikean elämäntilanteen väistyessä tai tunnetaitojen kehittyessä. Eläinkokeiden perusteella tiedetään, että myös masennuslääkkeet vaikuttavat aivojen muovautuvuuteen muun muassa lisäämällä hermokasvutekijöiden soluviestintää (1010 Casarotto PC, Girych M, Fred SM ym. Antidepressant drugs act by directly binding to TRKB neurotrophin receptors. Cell 2021;184:1299–313), mikä voi johtaa uusien synapsien muodostumiseen ja hermoverkostojen toiminnan kuntoutumiseen (99 Price RB, Duman R. Neuroplasticity in cognitive and psychological mechanisms of depression: an integrative model. Mol Psychiatry 2020;25:530–43.).
Viimeaikaiset kliiniset aivokuvantamistutkimukset ovat tuoneet uutta tietoa siitä, miten masennuksesta toipuminen ja eri masennushoitojen vaikutukset näkyvät aivojen rakenteessa. Tutkimuksissa on kartoitettu masennuspotilaiden ja verrokkien harmaan aineen tilavuutta tai aivokuoren paksuutta eri aivorakenteissa muun muassa vokselipohjaisella morfometrialla (VBM). Valkean aineen radastojen ominaisuuksia on kartoitettu diffuusiotensorikuvantamisella (DTI) ja traktografialla.
Masennuksesta toipumisen vaikutus aivojen rakenteeseen
Masennuksesta toipumisen vaikutusta aivojen rakenteeseen on tutkittu vertailemalla masentuneita, masennuksesta toipuneita (tai remissiovaiheessa olevia) ja terveitä verrokkeja poikittais- ja pitkittäistutkimuksissa. Poikittaistutkimuksissa on havaittu, että masennuksesta toipuneilla on suurempi harmaan aineen tilavuus hippokampuksessa (1111 Arnone D, McKie S, Elliott R ym. State-dependent changes in hippocampal grey matter in depression. Mol Psychiatry 2013;18:1265–72.), etuotsalohkon aivokuoren yläosassa, pihtipoimun etuosassa sekä päälakilohkon sisä- ja alaosissa (1212 Salvadore G, Nugent AC, Lemaitre H ym. Prefrontal cortical abnormalities in currently depressed versus currently remitted patients with major depressive disorder. NeuroImage 2011;54:2643–51.) masentuneisiin verrattuna. Toipuneiden ja terveiden verrokkien välillä ei havaittu rakenteellisia eroja.
Pitkittäistutkimuksissa on vastaavasti raportoitu, että 1–3 vuoden seurannan aikana masennuksesta toipuneilla harmaan aineen tilavuus kasvaa hippokampuksessa (1313 Frodl TS, Koutsouleris N, Bottlender R ym. Depression-related variation in brain morphology over 3 years: effects of stress? Arch Gen Psychiatry 2008;65:1156–65.,1414 Phillips JL, Batten LA, Tremblay P, Aldosary F, Blier P. A prospective, longitudinal study of the effect of remission on cortical thickness and hippocampal volume in patients with treatment-resistant depression. Int J Neuropsychopharmacol 2015;18:1–9.) sekä pihtipoimun etuosassa ja etuotsalohkon aivokuoren yläosassa (1313 Frodl TS, Koutsouleris N, Bottlender R ym. Depression-related variation in brain morphology over 3 years: effects of stress? Arch Gen Psychiatry 2008;65:1156–65.). Myös aivokuoren paksuus lisääntyy etuotsalohkon ala- ja keskiosissa sekä ohimolohkon alaosassa (1414 Phillips JL, Batten LA, Tremblay P, Aldosary F, Blier P. A prospective, longitudinal study of the effect of remission on cortical thickness and hippocampal volume in patients with treatment-resistant depression. Int J Neuropsychopharmacol 2015;18:1–9.) verrattuna edelleen masentuneisiin.
Masennuksesta toipumiseen on DTI-pitkittäistutkimuksissa liitetty myös valkean aineen radastojen rakenteellista eheyttä kuvaavien parametrien, kuten anisotropian tai diffuusiivisuuden, muutoksia etenkin limbisissä radastoissa, kuten pihtipoimua ja ohimolohkon sisäosia (mukaan lukien hippokampusta) yhdistävässä cingulum-radastossa sekä ohimolohkon etuosaa ja otsalohkon alaosaa yhdistävässä uncinate fasciculus (UF) -radastossa (1515 Bracht T, Jones DK, Müller TJ, Wiest R, Walther S. Limbic white matter microstructure plasticity reflects recovery from depression. J Affect Disord 2015;170:143–9.,1616 Doolin K, Andrews S, Carballedo A ym. Longitudinal diffusion weighted imaging of limbic regions in patients with major depressive disorder after 6 years and partial to full remission. Psychiatry Res Neuroimaging 2019;287:75–86.).
Laajassa traktografiatutkimuksessa todettiin, ettei masennuksesta toipumiseen liity koko aivoverkoston kattavia muutoksia valkeassa aineessa, mutta korkeammat anisotropian tasot aivosaaressa ja otsa-, ohimo- ja päälakilohkoissa sijaitsevien solmukohtien välillä olivat yhteydessä lievempään oirekuvaan (1717 Repple J, Mauritz M, Meinert S ym. Severity of current depression and remission status are associated with structural connectome alterations in major depressive disorder. Mol Psychiatry 2020;25:1550–8.). Tämä tukee käsitystä masennuksesta aivojen konnektiivisuuden häiriönä (disconnection syndrome), joka voi myös korjaantua masennuksesta toivuttaessa.
Masennuslääkityksen vaikutus aivojen rakenteeseen
Masennuslääkkeitä käytetään hyvin yleisesti masennuksen hoidossa, ja noin kaksi kolmasosaa potilaista saa niistä selvän hoitovasteen (11 Suomalaisen Lääkäriseuran Duodecimin ja Suomen Psykiatriyhdistys ry:n asettama työryhmä. Depressio. Käypä hoito -suositus. (siteerattu 27.9.2021). www.kaypahoito.fi). Masennuslääkkeiden vaikutuksia aivojen rakenteeseen on tutkittu ainakin selektiivisten serotoniinin takaisinoton estäjien (SSRI) sekä serotoniinin ja noradrenaliinin takaisinoton estäjien (SNRI) kohdalla.
Terveillä koehenkilöillä on havaittu, että 10 päivän SSRI-lääkitys lisää lumelääkkeeseen verrattuna harmaan aineen tilavuutta pihtipoimun takaosassa sekä päälakilohkon sisäosassa (precuneus) (1818 Kraus C, Ganger S, Losak J ym. Gray matter and intrinsic network changes in the posterior cingulate cortex after selective serotonin reuptake inhibitor intake. Neuroimage 2014;84:236–44.). Masennuspotilaiden pitkittäistutkimuksissa on raportoitu, että SSRI-lääkitys lisää 8–12 viikon seurannassa harmaan aineen tilavuutta hippokampuksessa (1111 Arnone D, McKie S, Elliott R ym. State-dependent changes in hippocampal grey matter in depression. Mol Psychiatry 2013;18:1265–72.) sekä etuotsalohkon ylä-sivuosissa ja orbitofrontaalisella aivokuorella (1919 Smith R, Chen K, Baxter L, Fort C, Lane RD. Antidepressant effects of sertraline associated with volume increases in dorsolateral prefrontal cortex. J Affect Disord 2013;146:414–9.,2020 Kong L, Wu F, Tang Y ym. Frontal-subcortical volumetric deficits in single episode, medication-naïve depressed patients and the effects of 8 weeks Fluoxetine treatment: a VBM-DARTEL study. PLoS One 2014;9:e79055.).
SNRI-lääkityksen on 10 viikon seurannassa puolestaan havaittu lisäävän harmaan aineen tilavuutta ja vähentävän aivokuoren paksuutta päälakilohkon sisä- ja ulko-osissa (precuneus, cuneus, kulmapoimu) verrattuna lumelääkkeeseen (2121 Yang J, Hellerstein DJ, Chen Y ym. Gray matter reorganization underpinnings of antidepressant treatment of persistent depressive disorder. Eur Neuropsychopharmacol 2021;43:129–38.,2222 Bansal R, Hellerstein DJ, Peterson BS. Evidence for neuroplastic compensation in the cerebral cortex of persons with depressive illness. Mol Psychiatry 2018;23:375–83.). On kuitenkin huomattavaa, että joissain SSRI- ja SNRI-lääkkeiden tutkimuksissa ei ole havaittu merkittäviä muutoksia aivorakenteissa (2323 Vythilingam M, Vermetten E, Anderson GM ym. Hippocampal volume, memory, and cortisol status in major depressive disorder: effects of treatment. Biol Psychiatry 2004;56:101–12.,2424 Suh JS, Minuzzi L, Cudney LE ym. Cerebral cortical thickness after treatment with desvenlafaxine succinate in major depressive disorder. Neuroreport 2019;30:378–82.). Näillä lääkkeillä ei DTI-tutkimuksissa myöskään ole raportoitu olevan pitkäkestoisia vaikutuksia valkean aineen radastoihin. Tiettyjen limbisten radastojen, kuten cingulumin, rakenteellisen eheyden on kuitenkin osoitettu ennustavan myöhempää positiivista hoitovastetta (2525 Davis AD, Hassel S, Arnott SR ym. White matter indices of medication response in major depression: a diffusion tensor imaging study. Biol Psychiatry Cogn Neurosci Neuroimaging 2019;4:913–24.,2626 Korgaonkar MS, Williams LM, Song YJ, Usherwood T, Grieve SM. Diffusion tensor imaging predictors of treatment outcomes in major depressive disorder. Br J Psychiatry 2014;205:321–8.).
Viime vuosina myös NMDA-antagonisti ketamiinin käyttö masennuksen hoidossa on yleistynyt. Ketamiinilla on nopea, jopa muutamassa tunnissa ilmenevä, mutta ohimenevä antidepressiivinen vaikutus. Pieniannoksista ketamiini-infuusiota käytetään nykyään hoitoresistentin masennuksen sekä vakavaan masennukseen liittyvän itsemurhavaaran hoidossa (11 Suomalaisen Lääkäriseuran Duodecimin ja Suomen Psykiatriyhdistys ry:n asettama työryhmä. Depressio. Käypä hoito -suositus. (siteerattu 27.9.2021). www.kaypahoito.fi,2727 Newport DJ, Carpenter LL, McDonald WM ym. Ketamine and other NMDA antagonists: early clinical trials and possible mechanisms in depression. Am J Psychiatry 2015;172:950–66.).
Ketamiinilla tarkoitetaan yleisesti sen kahden eri isomeerin (R(+) ja S(–)) sekoitusta, mutta hoidossa voidaan käyttää myös pelkkää S-ketamiinia. Uusimpien eläintutkimusten perusteella ketamiinin välitön vaikutus näyttää perustuvan sen aikaansaamaan hermokasvutekijöiden (BDNF) nopeaan synteesiin ja synaptogeneesiin aivoissa (88 Duman RS, Aghajanian GK. Synaptic dysfunction in depression: potential therapeutic targets. Science 2012;338:68–72.,1010 Casarotto PC, Girych M, Fred SM ym. Antidepressant drugs act by directly binding to TRKB neurotrophin receptors. Cell 2021;184:1299–313,2828 Autry AE, Adachi M, Nosyreva E ym. NMDA receptor blockade at rest triggers rapid behavioural antidepressant responses. Nature 2011;475:91–5.), ja sen vaikutuksia aivojen rakenteeseen on alettu tutkia myös ihmisillä.
Yksittäisen ketamiini-infuusion on masennuspotilailla 24 tunnin seurannassa havaittu lisäävän harmaan aineen tilavuutta alemmassa otsalohkopoimussa (2929 Dai D, Lacadie CM, Holmes SE ym. Ketamine normalizes the structural alterations of inferior frontal gyrus in depression. Chronic Stress 2020;4:1–10.) ja hippokampuksessa (3030 Abdallah CG, Jackowski A, Salas R ym. The nucleus accumbens and ketamine treatment in major depressive disorder. Neuropsychopharmacology 2017;42:1739–46.) ja vähentävän sitä tyvitumakkeiden accumbens-tumakkeessa (3030 Abdallah CG, Jackowski A, Salas R ym. The nucleus accumbens and ketamine treatment in major depressive disorder. Neuropsychopharmacology 2017;42:1739–46.). Nämä muutokset aivojen rakenteessa olivat kuitenkin vähäisiä, ja yhdessä myös S-ketamiinia koskevassa tutkimuksessa muutoksia ei todettu lainkaan (3131 Herrera-Melendez A, Stippl A, Aust S ym. Gray matter volume of rostral anterior cingulate cortex predicts rapid antidepressant response to ketamine. Eur Neuropsychopharmacol 2021;43:63–70.). DTI-tutkimuksessa huomattiin, että yksittäinen ketamiini-infuusio lisäsi 4 tunnin seurannassa anisotropiaa ventraalisessa (ILF) ja dorsaalisessa (superior longitudinal fasciculus, SLF) radastossa sekä limbisessä radastossa (UF) (3232 Sydnor VJ, Lyall AE, Cetin-Karayumak S ym. Studying pre-treatment and ketamine-induced changes in white matter microstructure in the context of ketamine’s antidepressant effects. Transl Psychiatry 2020;10:432.). Näissä tutkimuksissa myös osoitettiin, että pihtipoimun etuosan tilavuus sekä cingulum- ja SLF-radastojen anisotropia ennustivat merkitsevästi ketamiinin 24 tunnin hoitovastetta masennusoireisiin (3131 Herrera-Melendez A, Stippl A, Aust S ym. Gray matter volume of rostral anterior cingulate cortex predicts rapid antidepressant response to ketamine. Eur Neuropsychopharmacol 2021;43:63–70.,3232 Sydnor VJ, Lyall AE, Cetin-Karayumak S ym. Studying pre-treatment and ketamine-induced changes in white matter microstructure in the context of ketamine’s antidepressant effects. Transl Psychiatry 2020;10:432.).
Toistettujen ketamiini-infuusioiden (6 annosta 2–6 viikon aikana) on raportoitu saavan aikaan harmaan aineen tilavuuden kasvua mantelitumakkeessa ja hippokampuksessa (3333 Zhou Y-L, Wu F-C, Liu W-J ym. Volumetric changes in subcortical structures following repeated ketamine treatment in patients with major depressive disorder: a longitudinal analysis. Transl Psychiatry 2020;10:264.) sekä tyvitumakkeissa (mukaan lukien accumbens-tumake), talamuksessa ja keskiaivoissa (3434 Gallay CC, Forsyth G, Can AT ym. Six-week oral ketamine treatment for chronic suicidality is associated with increased grey matter volume. Psychiatry Res Neuroimaging 2021;317:111369.).
Ei-farmakologisen hoidon vaikutus aivojen rakenteeseen
Valtaosa masennuksen ei-farmakologisten hoitojen neuroplastisiteetin tutkimuksesta on tehty psykiatrisesta sähköhoidosta (electroconvulsive therapy, ECT). Sähköhoidossa johdetaan sähkövirtaa nukutetun potilaan aivokuorelle ulkoisten elektrodien kautta, mikä saa aikaan yleistyneen kouristuksen. Toistetulla sähköhoidolla on merkittävä antidepressiivinen vaikutus ja sitä pidetään vaikean, hoitoresistentin masennuksen tehokkaimpana hoitomuotona (3535 UK ECT Review Group. Efficacy and safety of electroconvulsive therapy in depressive disorders: a systematic review and meta-analysis. Lancet 2003;361:799–808.).
Masennuksen patogeneesiin ajatellaan liittyvän neuroplastisuuden heikentymistä.
Laajoissa tutkimuksissa ja meta-analyyseissä on osoitettu, että ECT lisää harmaan aineen tilavuutta laaja-alaisesti, voimakkaimmin subkortikaalisilla (aivokuorenalaisilla) alueilla (hippokampus, mantelitumake, talamus, tyvitumakkeet), mutta myös kortikaalisilla alueilla, etenkin pihtipoimun etuosassa, aivosaaressa ja ohimolohkolla (3636 Ousdal OT, Argyelan M, Narr KL ym. Brain changes induced by electroconvulsive therapy are broadly distributed. Biol Psychiatry 2020;87:451–61.,3737 Gbyl K, Videbech P. Electroconvulsive therapy increases brain volume in major depression: a systematic review and meta-analysis. Acta Psychiatr Scand 2018;138:180–95.). DTI-tutkimuksissa puolestaan on raportoitu ECT:n aikaansaamia anisotropian muutoksia frontolimbisissä (cingulum, forceps minor) ja dorsaalisissa (SLF) radastoissa (3737 Gbyl K, Videbech P. Electroconvulsive therapy increases brain volume in major depression: a systematic review and meta-analysis. Acta Psychiatr Scand 2018;138:180–95.,3838 Lyden H, Espinoza RT, Pirnia T ym. Electroconvulsive therapy mediates neuroplasticity of white matter microstructure in major depression. Transl Psychiatry 2014;4:e380.).
ECT:n rinnalle nousseen, useimmiten otsalohkon ylä-sivuosaan kohdennettavan transranskraniaalisen magneettistimulaation (TMS) on myös yhdessä tutkimuksessa havaittu lisäävän harmaan aineen tilavuutta pihtipoimun etuosassa, aivosaaressa, ohimolohkon yläosassa sekä päälakilohkolla (kulmapoimu) (3939 Lan MJ, Chhetry BT, Liston C, Mann JJ, Dubin M. Transcranial magnetic stimulation of left dorsolateral prefrontal cortex induces brain morphological changes in regions associated with a treatment resistant major depressive episode: an exploratory analysis. Brain Stimul 2016;9:577–83.).
Masennuksen psykologisten hoitomuotojen neuroplastisista vaikutuksista on toistaiseksi vähän tutkimusta. Psykoterapian, pääosin kognitiivisen käyttäytymisterapian (4–8 viikkoa), on kolmessa pienessä tutkimuksessa raportoitu lisäävän harmaan aineen tilavuutta tyvitumakkeissa (accumbens-tumake) (4040 Meng Y, Li H, Wang J, Xu Y, Wang B. Cognitive behavioral therapy for patients with mild to moderate depression: treatment effects and neural mechanisms. J Psychiatr Res 2021;136:288–95.) sekä otsalohkon keski- ja yläosassa (4141 Du X, Mao Y, Ran Q, Zhang Q, Luo Q, Qiu J. Short-term group cognitive behavior therapy contributes to recovery from mild depression: Evidence from functional and structural MRI. Psychiatry Res Neuroimaging 2016;251:53–9.,4242 Wang T, Huang X, Huang P, ym. Early-stage psychotherapy produces elevated frontal white matter integrity in adult major depressive disorder. PLoS One 2013;8:e63081.).
Tutkimusten arviointi ja yhteenveto
Magneettikuvaukseen (MK) pohjautuvat rakenteelliset aivokuvantamistutkimukset ovat viimeisen vuosikymmenen aikana osoittaneet, että masennuksesta toipuminen ja erityyppiset masennushoidot muovaavat aivojen rakennetta laaja-alaisesti. Rakenteellista muovautumista tapahtuu etenkin limbisillä alueilla (muun muassa hippokampus, talamus, accumbens-tumake) sekä myös frontotemporaalisilla alueilla (muun muassa pihtipoimun etuosa, etuotsalohkon ja ohimolohkon aivokuori, päälakilohkon alaosa) ja näitä yhdistävissä valkean aineen radastoissa (muun muassa cingulum, UF, ILF, SLF) (kuva 1).
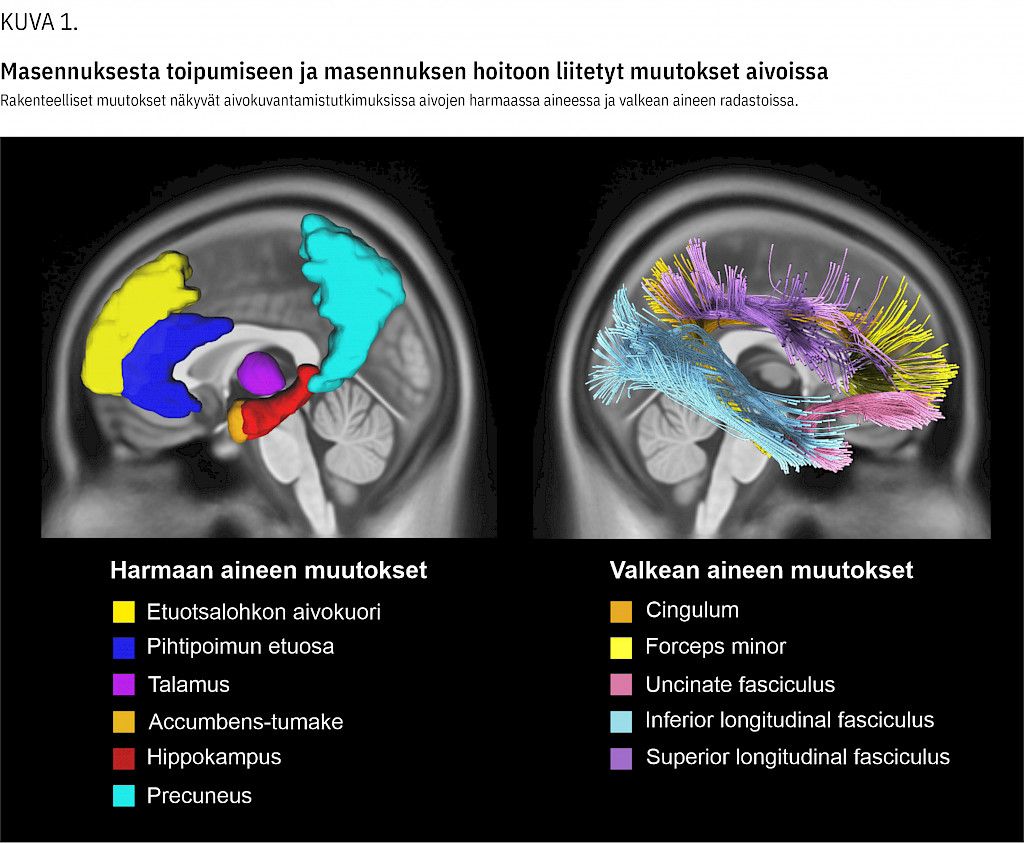
Samojen alueiden ja verkostojen tiedetään osallistuvan masennuksessa keskeisiin tunne-elämän ja ajattelun mekanismeihin, kuten negatiivisesti vinoutuneisiin havainto- ja tarkkaavaisuusprosesseihin, ajatusmalleihin (skeemoihin) ja muistoihin (99 Price RB, Duman R. Neuroplasticity in cognitive and psychological mechanisms of depression: an integrative model. Mol Psychiatry 2020;25:530–43.,4343 Disner S, Beevers C, Haigh EAP, Beck AT. Neural mechanisms of the cognitive model of depression. Nat Rev Neurosci 2011;12:467–77.).
Mikä mielenkiintoista, masennuksen eri hoitomuodot (SSRI, SNRI, ECT, TMS, KKT) näyttävät saavan aikaan pitkälti samanlaisia aivomuutoksia, joita tapahtuu myös spontaanissa toipumisessa. Tämä viittaa siihen, että vaikka hoitojen toimintaperiaatteet ovat erilaisia, niiden pitkäaikaisten vaikutusten taustalla voivat olla samat neuroplastiset ydinmekanismit, joiden kautta hermoverkostot voivat palautua varhaista herkkyyskautta muistuttavaan tilaan ja muovautua ympäristön ja kokemuksen kautta (4444 Castrén E. Neuronal network plasticity and recovery from depression. JAMA Psychiatry 2013;70:983–9.).
On hyvä huomioida, että tutkimuksissa havaitut muutokset aivojen rakenteessa ovat verrattain heterogeenisiä ja kooltaan melko pieniä. Lisäksi tutkimuksissa ilmenee metodologisia puutteita, jotka rajoittavat niistä saatavaa tietoa. Näitä ovat (i) käytettyjen otoskokojen pienuus, (ii) verrokkiryhmän ja satunnaistetun kontrolloidun tutkimusasetelman (RCT) puuttuminen, (iii) interventiojakson jälkeisen pitkittäisseurannan puuttuminen sekä (iv) epäselvä yhteys aivomuutosten ja käyttäytymisen muutosten (kliininen hoitovaste) välillä.
Rakenteelliset MK-tutkimukset eivät välttämättä paljasta kaikkia kliiniseltä kannalta merkittäviä muutosprosesseja, sillä niissä tarkastellaan anatomisesti verrattain karkeita makrotason muutoksia, eivätkä ne tuota tietoa hermoverkkojen toiminnallisesta uudelleenorganisoitumisesta ja konnektiivisuudesta. Tässä toiminnalliset magneettikuvantamistutkimukset olisivat avainasemassa (4545 Kaiser RH, Andrews-Hanna JR, Wager TD, Pizzagalli DA. Large-scale network dysfunction in major depressive disorder: a meta-analysis of resting-state functional connectivity. JAMA Psychiatry 2015;72:603–11.).
Eri hoitomuotojen, kuten kognitiivisen käyttäytymisterapian ja sähkö- tai lääkehoidon, yhdistämisen aikaansaamasta neuroplastisiteetista tiedetään myös hyvin vähän, vaikka multimodaaliset hoidot tiedetään tehokkaiksi ja niiden avulla voitaisiin mahdollisesti saavuttaa myös voimakkaampia ja pysyvämpiä neuroplastisia muutoksia (4646 Wilkinson ST, Holtzheimer PE, Gao S, Kirwin DS, Price RB. Leveraging neuroplasticity to enhance adaptive learning: the potential for synergistic somatic-behavioral treatment combinations to improve clinical outcomes in depression. Biol Psychiatry 2019;85:454–65.).
Emma Oksanen
PsK
Helsingin yliopisto, psykologian ja logopedian osasto
Aleksi J. Sihvonen
Multimodaaliset hoidot tiedetään tehokkaiksi.
LT, tutkijatohtori
Helsingin yliopisto, psykologian ja logopedian osasto, kognitiivisen aivotutkimuksen yksikkö ja
University of Queensland, School of Health and Rehabilitation Sciences, Queensland Aphasia Research Centre ja UQ Centre for Clinical Research
Hasse Karlsson
LT, FM, integratiivisen neurotieteen ja psykiatrian professori, ylilääkäri
Turun yliopisto ja VSSHP, psykiatria
Teppo Särkämö
PsT, dosentti, neuropsykologian apulaisprofessori
Helsingin yliopisto, psykologian ja logopedian osasto, kognitiivisen aivotutkimuksen yksikkö
Kirjoitus on julkaistu aiemmin Lääkärilehden verkkosivuilla.






